
Թեստ


Սովորել՝ Ջրածին։ Հասկացողություն թթուների և աղերի մասին։
Էջ՝ 129-133

Ջրածինը (Hydrogenium` լատիներեն ջուր ծնող) պարբերական համակարգի առաջին պարբերության՝ առաջին խմբի, մեկ կարգաթվով տարրն է:

ջրածին տարրի նշանը
Ջրածնի ատոմն ունի ամենապարզ կառուցվածքը` մեկ դրական լիցքով միջուկի շուրջը սփռված է մեկ էլեկտրոն:

ջրածնի ատոմի կառուցվածքը
Միացություններ առաջացնելիս ջրածինը հիմնականում ցուցաբերում է մետաղական հատկություն, այսինքն՝ տալիս է մեկ էլեկտրոն և ձեռք է բերում +1 լիցք:
H0−1e→H+
Իսկ որոշ պայմաններում ոչ մետաղական հատկություն` ընդունում է էլեկտրոն (օրինակ՝ մետաղների հետ առաջացած միացություններում) և ձեռք բերում −1օքսիդացման աստիճան:
H0+1e−→−H−
Միացությունների ձևով ջրածինը չափազանց տարածված տարր է: Նա կազմում է ջրի զանգվածի 11 %-ը, մտնում է բոլոր բուսական` մրգերի, բանջարեղենների, թթուների, և կենդանական նյութերի` ճարպերի, սպիտակուցների, ածխաջրերի, նավթի, և շատ այլ հանքային նյութերի բաղադրության մեջ:
Նա կազմում է արեգակի և աստղերից շատերի զանգվածի կեսից ավելին: Արեգակնային համակարգի ամենամեծ մոլորակը` Յուպիտերը, համարյա լրիվ կազմված է ջրածին քիմիական տարրից: Ցածր ջերմաստիճանի և շատ բարձր ճնշման պատճառով ջրածինն այդ մոլորակի վրա գտնվում է պինդ վիճակում:
Ջրածին տարր պարունակող ցանկացած միացություն պարունակում է ջրածնի երկու իզոտոպ` պրոտիում ( 99,98) և դեյտերիում (0,02): Աննշան քանակությամբ հանդիպում է նաև երրորդ իզոտոպը` տրիտիումը:

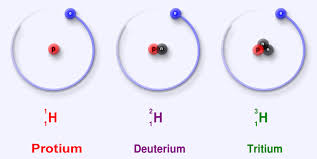
ջրածնի իզոտոպները
Ջրածին տարրն առաջացնում է ջրածին պարզ նյութը՝
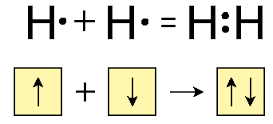
Ջրածնի մոլեկուլի բանաձևն է՝ H2, հարաբերական մոլեկուլային զանգվածը՝ 2,016 (կլորացված 2), մոլային զանգվածը՝ 2 գ/մոլ՝
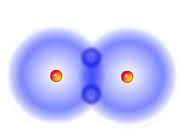
ջրածնի մոլեկուլի մոդելը
Ջրածինը բնության մեջ ազատ վիճակում հանդիպում է չնչին քանակով՝ գլխավորապես մթնոլորտի վերին շերտերում: Երբեմն, այն երկրի ընդերքից դուրս է գալիս այլ գազերի հետ հրաբխային ժայթքումների, ինչպես նաև նավթի արդյունահանման ժամանակ:
ՀԱՐՑԵՐ, ՎԱՐԺՈՒԹՅՈՒՆՆԵՐ ԵՎ ԽՆԴԻՐՆԵՐ

Дата: 16 марта, 2024Автор: varsenikgrigoryanblog0 Комментарии
Սովորել՝ Մետաղների օքսիդներ ՝ Հիմնային օքսիդներ ։ Հիմքեր։
Էջ ՝ 105-108
Մետաղների օքսիդներում թթվածին տարրի ատոմը (ատոմները) միացած է մետաղ տարրի ատոմի (ատոմների) հետ:
Օրինակ՝ CuO,MgO,ZnO,Na2O,Cr2O3 և այլն:
Մետաղների օքսիդները սովորական պայմաններում պինդ նյութեր են:
Մետաղների օքսիդները, որոնց համապատասխանում են հիմքեր, անվանում են հիմնային օքսիդներ:
Օրինակ՝ CuO→Cu(OH)2,Na2O→NaOH,MgO→Mg(OH)2 և այլն:
Եթե մետաղը տարբեր օքսիդացման աստիճան է դրսևորում, ապա որպես կանոն ցածրագույն օքսիդացման աստիճաներին են համապատասխանում հիմնային օքսիդներ:
Օրինակ՝ քրոմը առաջացնում է երեք օքսիդ՝ Cr+2O,Cr+32O3,և Cr+6O3,, որոնցից միայն Cr+2O է հիմնային օքսիդ:
Պարբերական համակարգի I Ա և II Ա (բացի բերիլիումից և մագնեզիումից) մետաղների օքսիդները փոխազդում են ջրի հետ՝ առաջացնելով համապատասխան լուծելի հիմքեր:
Օրինակ՝ Na2O+H2O=2NaOHCaO+H2O=Ca(OH)2
Հիմքերը բարդ նյութեր են, որոնք կազմված են մետաղի ատոմներից և մեկ կամ մի քանի հիդրոքսոներից՝ 0Hխմբից:

Պատասխանել հարցերին
5)Ո՞ր ինդիկատորի գույնն է նույնը և ջրում, և՛ ալկալու լուծույթում։
Էջ ՝ 105-108
Մետաղների օքսիդներում թթվածին տարրի ատոմը (ատոմները) միացած է մետաղ տարրի ատոմի (ատոմների) հետ:
Օրինակ՝ CuO,MgO,ZnO,Na2O,Cr2O3 և այլն:
Մետաղների օքսիդները սովորական պայմաններում պինդ նյութեր են:
Մետաղների օքսիդները, որոնց համապատասխանում են հիմքեր, անվանում են հիմնային օքսիդներ:
Օրինակ՝ CuO→Cu(OH)2,Na2O→NaOH,MgO→Mg(OH)2 և այլն:
Եթե մետաղը տարբեր օքսիդացման աստիճան է դրսևորում, ապա որպես կանոն ցածրագույն օքսիդացման աստիճաներին են համապատասխանում հիմնային օքսիդներ:
Օրինակ՝ քրոմը առաջացնում է երեք օքսիդ՝ Cr+2O,Cr+32O3,և Cr+6O3,, որոնցից միայն Cr+2O է հիմնային օքսիդ:
Պարբերական համակարգի I Ա և II Ա (բացի բերիլիումից և մագնեզիումից) մետաղների օքսիդները փոխազդում են ջրի հետ՝ առաջացնելով համապատասխան լուծելի հիմքեր:
Օրինակ՝ Na2O+H2O=2NaOHCaO+H2O=Ca(OH)2
Հիմքերը բարդ նյութեր են, որոնք կազմված են մետաղի ատոմներից և մեկ կամ մի քանի հիդրոքսոներից՝ 0Hխմբից:

Պատասխանել հարցերին
5)Ո՞ր ինդիկատորի գույնն է նույնը և ջրում, և՛ ալկալու լուծույթում։

1)Հեղուկները լողում են և սուզվում
Հեղուկները նույնպես կարող են մնալ ջրի երեսին կամ իջնել ներքև։ Դա կախված է խտություն կոչվող մեծությունից: Փոքր խտությամբ նյութը ավելի քիչ կշիռ ունի, քան նույն ծավալով ավելի մեծ խտությամբ մեկ այլ նյութ։ Որևէ առարկա կամ հեղուկ կմնա իրենից ավելի մեծ խտություն ունեցող հեղուկի մեկերևույթին:
Անհրաժեշտ են ՝ գունավոր ջուր, օշարակ, բուսայուղ, լողալու համար առարկաների խումբ, մեծ տարա։
1) Զգուշությամբ օշարակը լցրո՛ւ տարայի մեջ մեկ քառորդ չափով: Ավելի հեշտ կլցնես՝ օգտագործելով գդալի հակառակ կողմը:
2)Դանդաղորեն տարայի մեջ լցրո՛ւ նույնչափ բուսայուղ, այնուհետև ավելացրու նույնչափ գու- նավորված ջուր:
3)Երեք տեսակի հեղուկները բաժանվում են առանձին շերտերի և լողում մեկը մյուսի վրա։ Այժմ ավելացրո՛ւ լողալու համար նախատեսված առարկաները։
2)Հեղուկները խառնվու՞մ են , թե ոչ
Որոշ հեղուկներ հեշտ է գունավորել, մյուսները՝ ոչ։ Տե՛ս, թե ինչպես է բուսայուղը «դիմադրում», երբ փորձում ես երանգավորել սննդի գունանյութով։ Սա նշանակում է՝ բուսայուղը չի թողնում, որ գունանյութը խառնվի իրեն։ Պարզի՛ր, թե ինչ է կատարվում գունանյութի հետ, երբ խառնվում է ջրին։
Անհրաժեշտ են՝ սննդային գունանյութ, հեղուկաչափ, գդալ, կաթոցիկ, ջուր, բուսայուղ։
1)Հեղուկաչափի մեջ լցրո՛ւ ջուր և մի փոքր բուսայուղ ավելացրո՛ւ: Երկու առանձին շերտեր են առաջանում, քանի որ բուսայուղն ու ջուրը չեն խառնվում:
2)Զգուշորեն մի քանի կաթիլ գունանյութ ավելացրո՛ւ հեղուկաչափի մեջ: Կաթիլները լողում են բուսայուղի մեջ:
3)Գդալով փորձի՛ր կաթիլները հրել ջրի մեջ։ Ջրում հայտնվելուն պես ի՞նչ է կատարվում հեղուկները խառնվո՞ւմ են,թե՞ ոչ։
3)Պայքարի’ր կրակի դեմ
Վառի՛ր մի մոմ և առանց փչելու կամ բոցին դիպչելու, ասես հրաշքով, հանգցրո՛ւ: Սա հնարավոր է, որովհետև իրերն այրվում են, երբ թթվածին են ստանում օդից։ Ընդհատի՛ր թթվածնի մատակարարումը, և կրակը կմարի:
Անհրաժեշտ են՝ լուցկի, մոմ, քացախ, գդալ, ապակե աման, պլաստիլին, սոդա։
1)Պլաստիլինի օգնությամբ ամրացրո՛ւ մոմը ամանի հատակին:
2)Սոդան լցրո՛ւ մոմի շուրջը:
3) Մեծերից մեկի օգնությամբ վառի՛ր մոմը լուցկիով:
4) Ավելացրո՛ւ մի քիչ քացախ։ Սոդան սկսում է փրփրել։
5)Հանգիստ սպասի՛ր։ Հանկարծ չգիտես ինչու, կրակը մարում է:
6)Փորձի՛ր նորից վառել մոմը։ Դա անհնարին է:
Ի՞ նչ է կատարվում փորձի ընթացքում։
Քացախը և սոդան ին՞չ խոչընդոտ են առաջացնում։
4)<Ջերմուկ>
«Ջերմուկ» հանքային ջրում լուծված աղերի գումարային պարունակությունը (ընդհանուր հանքայնացումը) հավասար է 4,1 գ/դմ3 ։
Քանի՞ գրամ լուծված աղեր են պարունակում 200մլ տարողությամբ մեկ բաժակ < Ջերմուկում>։
1)Տվե՛ք ջրածին քիմիական տարրի բնութագիրը` ըստ տևյալ պլանի.
ա) քիմիական նշանը,
H
բ) հարաբերական ատոմային զանգվածը,
1,00797
գ) դիրքը պարբերական համակարգում,
առաջին պարբերություն, առաջին խումբ
2)Բնութագրե՛ք ջրածին պարզ նյութը` ըստ հետևյալ պլանի
ա) քիմիական բանաձևը,
թ) մոլեկուլի կառուցվածքը,
գ) հարաբերական մոլեկուլային զանգվածը,
դ) մոլային զանգվածը:
3)Տիեզերքում ու Երկրագնդի մթնոլորտի վերին րում ո՞ր քիմիական տարրն է ամենատարածվա տրե՛ք ճիշտ պատասխանը
ա) թթվածին,
բ) ազոտ,
գ) ջրածին,
դ) հելիում:
4)Հաշվե՛ք տրված զանգվածներով ջրածին նյութի քանակը (մոլ).
ա)1 գ
բ)4 գ
q) 10 գ
Պատ.`ա) 0,5 մոլ H2
բ) 2 մոլ H2
գ) 5 մոլ H2
5)Հաշվե՛ք ջրածին տարրի զանգվածային բաժինը (%) մեթանի CH4 մոլեկուլում
Պատ.՝ 25% H:
6)Հաշվե՛ք ջրածնի ատոմների թիվն 9 գ ջրում:
Պատ.՝ 6, 2 • 10{23}
7)Գրել ռեակցիաների տեսակները
ա) H2 +CL2= 2HCl ?
բ)Fe+ 2HCl= Fe Cl2 + H2 ?
Գ) 2H2O=2H2+O2 ?
Սովորել՝ Թթվածնի քիմիական հատկությունները։
Էջ՝ 97-101

Թթվածինը քիմիապես ակտիվ նյութ է: Այն փոխազդում է պարզ նյութերի հետ՝ ոչ մետաղների և մետաղների, ինչպես նաև` բարդ նյութերի:
Կարևոր է նշել, որ թթվածնի պակասի դեպքում ածխի այրումից առաջանում է խիստ վտանգավոր գազ՝ ածխածնի (II) օքսիդ (CO՝ շմոլ գազ).
2C+O2→2CO↑
Ամենակարևորը թթվածինը նպաստում է այրմանը և շնչառությանը։ Այն մեծ չափով նպաստում է մետալուրգիական գործընթացներին՝ թուջի, պողպատի, ինչպես նաև գունավոր մետաղների (Cu, Zn, Sn, Au) արտադրության համար։ Բժշկության մեջ ծանր հիվանդներին տալիս են թթվածին։ Թթվածին ծախսվում է մետաղների կտրման և եռակցման ժամանակ, սուզանավերում, տիեզերանավերում, ջրի տակ աշխատող մարդկանց համար։
Գործնական աշխատանք
Լաբորատոր փորձ ՝ 1
Լաբորատոր փորձ ՝ 2
Լաբորատոր փորձ ՝ 3
Լաբորատոր փորձ ՝ 4
Լաբորատոր փորձ ՝ 5

Սովորել՝ Թթվածնի ֆիզիկական հատկությունները և ստացումը։
Թթվածինը սովորական պայմաններում անգույն, անհոտ, անհամ գազ է:
Ջրում քիչ է լուծվում, սովորական պայմաններում մեկ լիտր ջրում 30 մլ թթվածին է լուծվում ( 100 ծավալ ջրում՝ 3 ծավալ թթվածին): Ջերմաստիճանը իջեցնելիս լուծելիությունը մեծանում է: Օրինակ՝ 100ծավալ սառցաջրում (0°𝐶) 5 ծավալ թթվածին է լուծվում:
Թթվածնի խտությունը 0°𝐶-ում և 101 կՊա ճնշման պայմաններում 1,43 գ/լ է, օդից ծանր է 1,11 անգամ: Թթվածինը եռում է −183°𝐶-ում, իսկ պնդանում է −219°𝐶-ում՝ առաջացնելով բաց երկնագույն բյուրեղներ:
Թթվածնի ստացումը
Առաջին անգամ թթվածին ստացել են սնդիկի օքսիդի (𝐻𝑔𝑂) քայքայումից:
2𝐻𝑔𝑂=𝑡°2𝐻𝑔+Օ2
Արդյունաբերության մեջ թթվածին ստանում են՝
1. Հեղուկ օդից
2. Ջրի էլեկտրոլիզից
2𝐻2Օ=2𝐻2+𝑂2
Լաբորատորիայում հնարավոր է ստանալ թթվածին՝ այդ տարրը պարունակող բարդ նյութերը քայքայելով:
1. Կալիումի պերմանգանատի քայքայումից՝
2𝐾𝑀𝑛𝑂4=𝑡°𝐾2𝑀𝑛𝑂2+𝑀𝑛𝑂4+𝑂2
2.Կալիումի քլորատի քայքայումից՝
2𝐾𝐶𝑙𝑂3=𝑡°,𝑀𝑛𝑂22𝐾𝐶𝑙+3𝑂2
3. Ջրածնի պերօքսիդի քայքայումից՝
2𝐻2𝑂2=2𝐻2𝑂+𝑂2
4. Կալիումի նիտրատի քայքայումից՝
2𝐾𝑁𝑂3=𝑡°2𝐾𝑁𝑂2+𝑂2
Անջատվող թթվածինը հայտնաբերում են առկայծող մարխով՝ այն թթվածնով փորձանոթի մեջ մտցնելիս բռնկվում է:

Նոր թեմա- Թթվածին։

ՀԱՐՑԵՐ, ՎԱՐԺՈՒԹՅՈՒՆՆԵՐ ԵՎ ԽՆԴԻՐՆԵՐ
ա) ո՞րն է թթվածին տարրի քիմիական նշանը,
Թթվածնի քիմիական նշանը O:
բ) որքա՞ն են թթվածնի հարաբերական ատոմային և մոլային զանգվածները,
Ar=16
M(O2)=32
գ) ո՞րն է թթվածին տարրի կարգաթիվը,
8
դ) քանի՞ էլեկտրոն է առկա թթվածնի ատոմի արտաքին էներգիական մակարդակում,
Էներգիական մակարդակների թիվը հավասար է պարբերության համարին 2:
Օդի թթվածինը հիմնականում ծախսվում է նյութերի այրման, օքսիդացման, օրգանական նյութերի նեխման և կենդանի օրգանիզմի շնչառության:
16×2,5=40
16×3=48
48×3=144
144+40=188
Խմբային աշխատանք
Օգտվելով տվյալներից՝ յուրաքանչյուր աշակերտ պետք է որոշի.
ա) թթվածին տարրի զանգվածն իր օրգանիզմում,
բ) թթվածնի ծավալը դասասենյակում:
Առաջադրանք
Սլաքների օգնությամբ ցույց տվեք թթվածնի շրջապտույտը բնության մեջ.
